近期,Mass General Brigham評選出了第六屆細胞與基因療法“顛覆性技術”Top12,認為這些技術將在未來幾年內對醫療健康產生重要的影響。其中不斷取得突破性進展的“干細胞療法治療糖尿病”技術位列其中,同時還包括細胞基因療法治療帕金森、通用型CAR-T療法等。
全球糖尿病人數或將達到7億
糖尿病是一種以高血糖為特征的慢性代謝疾病,當胰腺產生不了足夠的胰島素或者人體無法有效地利用所產生的胰島素時,就會出現糖尿病。近年來,全球糖尿病的患病人數不斷攀升,全球平均增長率為51%,按照這個趨勢,預計到2045年全球將有7億糖尿病患者!
目前臨床上糖尿病類型的主要分為1型糖尿病和2型糖尿病,治療方式主要是藥物治療,分為口服藥物和注射胰島素。多數需要不間斷地長期用藥。糖尿病的并發癥難以控制,給患者身體和生活都帶來嚴重的負擔。
干細胞,尤其是間充質干細胞具有低免疫原性和多能性等特性,已用于多種疾病的治療研究。近年來,科研人員們正在開發用來治療糖尿病的干細胞療法,希望能達到一次治療長期有效的結果。
干細胞治療糖尿病的策略
干細胞療法的策略之一就是使干細胞分化成可以分泌胰島素的胰島樣細胞。
體內胰腺細胞發育的過程和信號通路已經研究的較為清楚,基于這些研究理論,近幾年來研究者們利用不同的激素和生長因子去刺激或者抑制相應的信號通路,在體外利用人的多能干細胞分化成胰腺祖細胞,繼而產生能分泌胰島素的β樣細胞,已經取得了相當多的進展。多個實驗室目前都關注在產生成熟的功能齊全的β樣細胞和胰島細胞,希望將他們移植到人體內可以取代人類胰島的功能。
干細胞治療糖尿病另一種重要的策略就是通過動脈導管直接移植成體干細胞到人類的胰島中,使干細胞在胰腺微環境的誘導下定向分化為正常的成熟胰島樣細胞并分泌胰島素,達到治療糖尿病的目的。
干細胞治療糖尿病的優勢
基于目前干細胞治療糖尿病的研究,顯示的分子機制主要集中在以下幾個方面:
(1)干細胞具有多向分化潛能,干細胞通過誘導能夠分化成為胰島β細胞;
(2)干細胞具有強大的旁分泌作用,包括干細胞與胰島共移植增強胰島存活,
(3)干細胞的免疫抑制作用,抑制T細胞增殖,降低炎癥反應;
(4)干細胞分泌的細胞因子,能夠修復受損細胞,促進細胞增殖分化,具有抗氧化能力,保護內源性β 細胞,從而改善了胰島 β細胞的功能。

全球數百項臨床試驗進行中
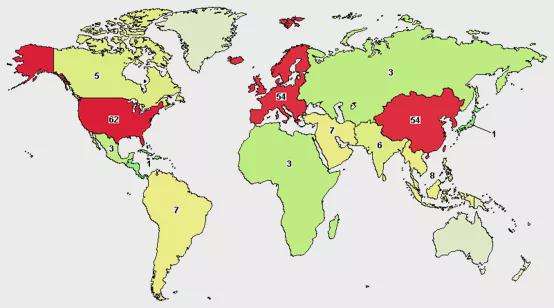
截止到2021年6月,根據在美國國立衛生研究院(NIH)的臨床試驗注冊網站(clinicaltrials.gov)的數據,全球正在開展的糖尿病相關干細胞治療臨床試驗共計230項,82項已完成,其中我國注冊項目54項,10項已完成,這些項目主要涉及1型糖尿病、2型糖尿病以及糖尿病血管病變、神經病變、糖尿病足等糖尿病并發癥的治療。
2020年10月,一項干細胞治療糖尿病的臨床研究入圍國家科技部“干細胞及轉化研究”重點專項,項目名稱為《人GLP-1和FGF21雙因子高表達自體脂肪間充質干細胞輸入治療2型糖尿病臨床研究》,這是國內繼2016年“干細胞及轉化研究”重點項目《利用體內微環境實現糖尿病中胰島細胞轉分化再生的機制研究》獲批之后的又一個關于干細胞治療糖尿病的專項。
多項針對研究1型糖尿病和2型糖尿病的臨床研究結果顯示干細胞治療糖尿病具有一定的有效性和安全性,已經初步取得了比較好的效果。
未來的機遇與挑戰
糖尿病作為困擾人類社會最為嚴重的一種慢性病,開發出高效安全的治療方法尤為緊迫和關鍵,相比于傳統的化學藥物和注射胰島素治療、器官移植等,干細胞療法獨特的優勢顯得尤為突出,可以有效避免免疫排斥,治療來源缺乏等問題,并且越來越多的臨床研究證實了干細胞療法的有效性和安全性。
未來,仍然有問題需要解決,例如探討干細胞分化胰島細胞的復雜性,不同組織來源以及不同類型的干細胞治療效果的差異;臨床應用上,干細胞制備工藝過程中的質量控制,干細胞輸入的次數、頻率、數量等都有待進一步的研究和確定。
隨著研究的不斷深入和臨床技術的不斷成熟,相信干細胞治療糖尿病的光明前景會被更加廣泛的證實,并為飽受糖尿病折磨的病人帶來重生。



